近日,国际癫痫领域顶级期刊《Epilepsia》在线发表了复旦大学人类表型组研究院、医学遗传研究院安宇团队,联合复旦大学附属儿科医院王艺团队等多家单位的研究论文,题为“Decoding epilepsy's molecular blueprint: Machine learning unravels transcriptomic subtypes and regulatory networks”。该研究通过对大规模耐药性癫痫患者手术脑组织的转录组测序,利用机器学习方法,首次揭示了独立于传统病理分类的两种分子亚型,并基于分子亚型的关键调控通路构建了分子分型预测模型,为癫痫分型和精准诊疗提供了全新的框架。
研究背景
耐药性癫痫影响着约三分之一的癫痫患者,其背后的分子机制异质性极高,长期未得到清晰定义。目前的癫痫分类主要依赖临床症状和组织病理学特征,例如局灶性皮质发育不良(FCD)虽被细分为不同亚型,但其背后的分子多样性尚不明确。由于人脑病理组织样本获取困难且遗传背景复杂,从分子层面系统解析癫痫异质性的研究十分有限。近年来,机器学习为疾病亚型的重新定义提供了强大的数据驱动手段,但鲜有研究将其应用于改进癫痫的分子分型。
研究方法与核心发现
在该项研究中,安宇、王艺团队联合对95例耐药性癫痫患者手术切除的153个脑组织样本(包括病灶及周边组织)进行了全面的RNA测序分析。通过无监督聚类,研究团队发现了两种基于转录组的分子亚型,它们与传统病理学分类(如FCD不同亚型、海马硬化等)并不完全吻合,提示存在一种新的、基于分子特征的癫痫分类基础。在排除脑区、病理等协变量的影响后,根据细胞组成差异(神经元比例高低),这两种亚型被命名为“高神经元组(HN)”和“低神经元组(LN)”。
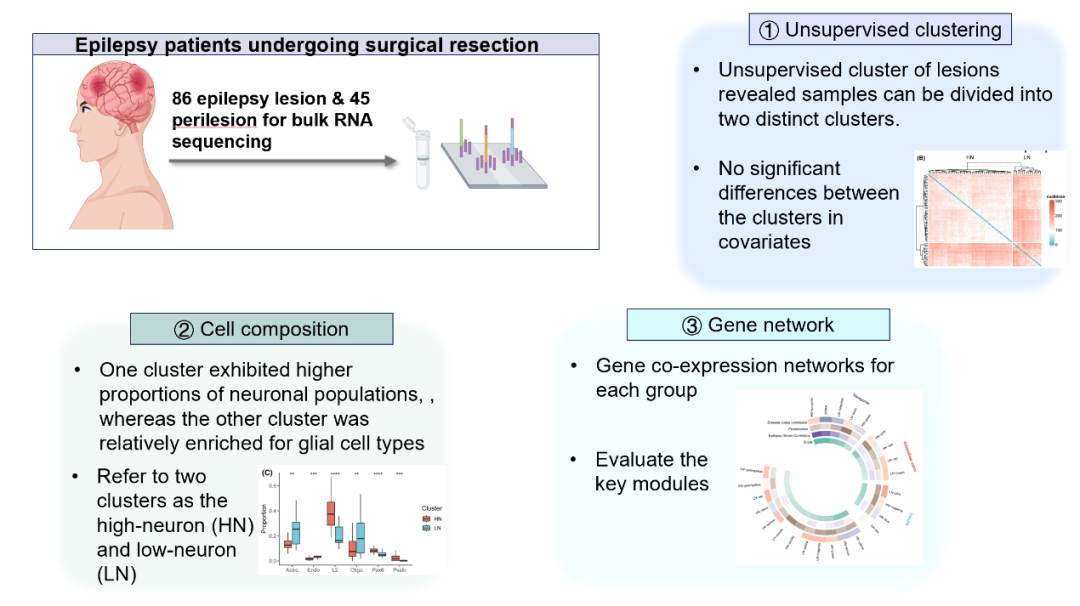
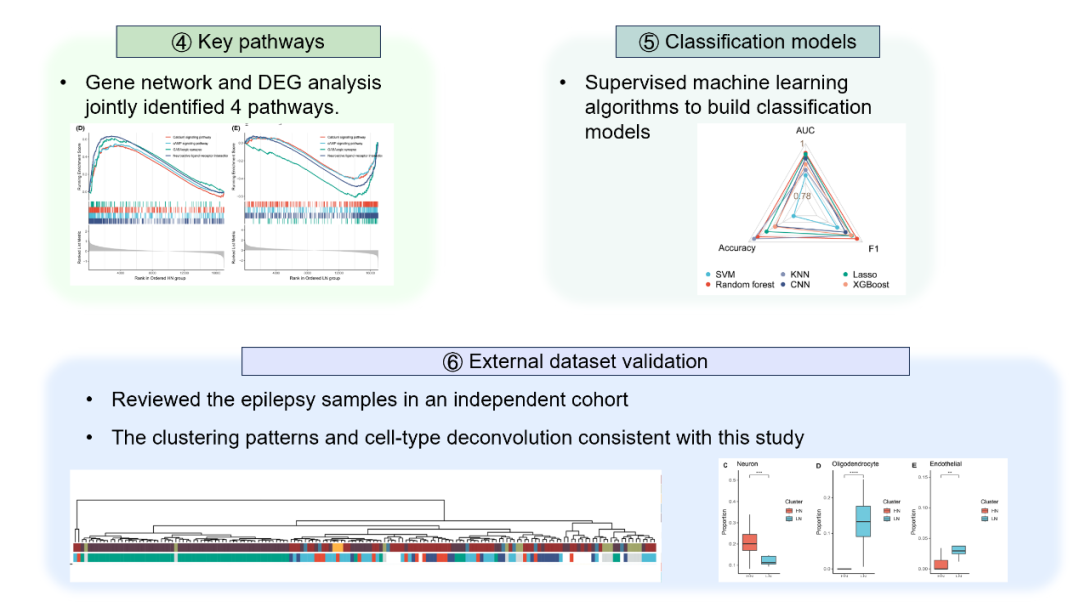
图 1 研究示意图
对这两种亚型的病理报告进行分析,HN组的FCD(53.6%)和皮层结构异常(12.5%)相比于LN组更高。进一步通过加权基因共表达网络分析(WGCNA)和通路富集分析,研究团队锁定了区分这两种亚型的四个关键失调通路:神经活性配体-受体相互作用;cAMP信号通路;GABA能突触;钙信号通路。值得注意的是,这四个通路在HN组和LN组中呈现出完全相反的调控模式(在HN组中上调,在LN组中下调),揭示了两种亚型可能代表了不同的神经元兴奋性调节状态。
基于这四个关键通路的基因集,研究团队构建了六种机器学习分类模型。其中,随机森林模型表现最优,该模型在一个独立的外部数据集中也得到了有效验证,被预测为LN组的样本同样显示出更低的神经元比例,证实了该分型框架的稳健性和普适性。
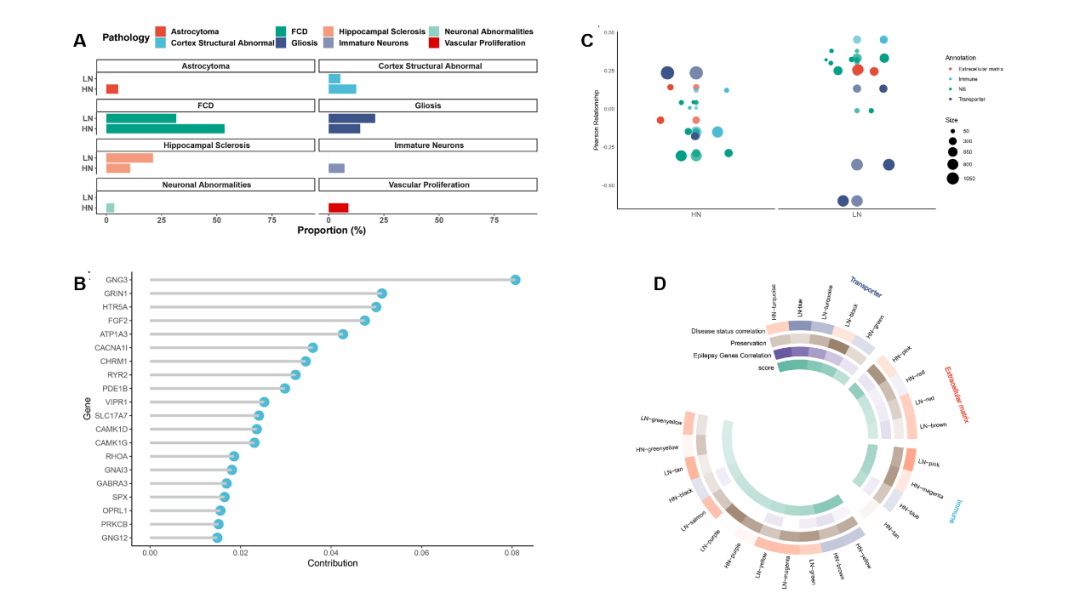
图 2 两个亚组的病理与基因表达网络分析。(A) 病灶簇中病理信息比例的条形图。横轴是组中出现的每种病理的比例。颜色代表病理。(B) 通过机器学习模型分析能够区分不同分组的特征,图中显示了对模型贡献最大的10个基因。(C) 比较各组疾病状态与模块特征基因之间的皮尔逊相关系数。通过基因富集分析,基因模块根据其生物学功能进行注释。圆圈大小表示模组中的基因数量。(D)圆形热力图,显示每个小组在三个方面的得分。从内部到外部:疾病状态与模块特征基因之间的皮尔逊相关系数(蓝色和红色)、模块的保存秩(青色)、模块与报告的癫痫相关基因之间的基因重叠比率(紫色),以及通过最小最大归一化法进行标度的最终得分(绿色)。基因模块名称及其生物功能显示在外部。
研究结论与意义
该研究首次通过数据驱动的方式,系统描绘了耐药性癫痫的转录组学蓝图,成功鉴定出两种超越传统病理分类的分子亚型。研究发现,四个关键的突触信号通路在两种亚型中的反向调控,可能是其不同病理生理机制的核心。基于此构建的机器学习分类模型,不仅为理解癫痫的分子异质性提供了新视角,更可能为未来开发针对特定分子亚型的靶向疗法、以及术前辅助判断癫痫病理类型提供重要的理论基础。
该研究是复旦大学多团队紧密合作的成果。复旦大学人类表型组研究院、医学遗传研究院安宇副教授,复旦大学附属儿科医院王艺教授为本文共同通讯作者。2021级硕士生翁艳平、马娱为共同第一作者。该研究获得了国家重点研发计划、宁波市科技项目、上海市科技重大专项国际人类表型组计划等项目的资助。
论文链接(点击阅读原文即可跳转):https://doi.org/10.1002/epi.70161






