乳腺癌的精准分型对于治疗方案的选择至关重要,而单一或单类型生物标志物的检测容易导致假阳性结果。然而,传统多重检测方法常受限于荧光光谱重叠和编码载体生物相容性差,难以充分发挥多重分析的潜能。此外,常规解码方法难以在单细胞水平上精确破译真正的靶点识别事件,尤其是多色荧光团标记靶标的空间信息。
近日,复旦大学人类表型组学研究院宓现强教授团队开发了一种四面体DNA纳米线为载体的复合荧光编码技术,融合MATLAB共定位解码方法,根据分子指纹实现三种乳腺细胞类型的逻辑区分。研究成果“Fluorescence Encoding Technology Based Tetrahedral Nano-string for Logic Identification of Breast Cancer Cells”发表于Materials Today Bio(中科院1区和JCR Q1区TOP期刊,IF=10.2)。该工作在活细胞层面实现了对两类不同分子(miRNA与膜蛋白)的逻辑编码与协同识别,为精准医学中多靶标协同诊断提供了一种灵活且可推广的解决方案。

技术设计
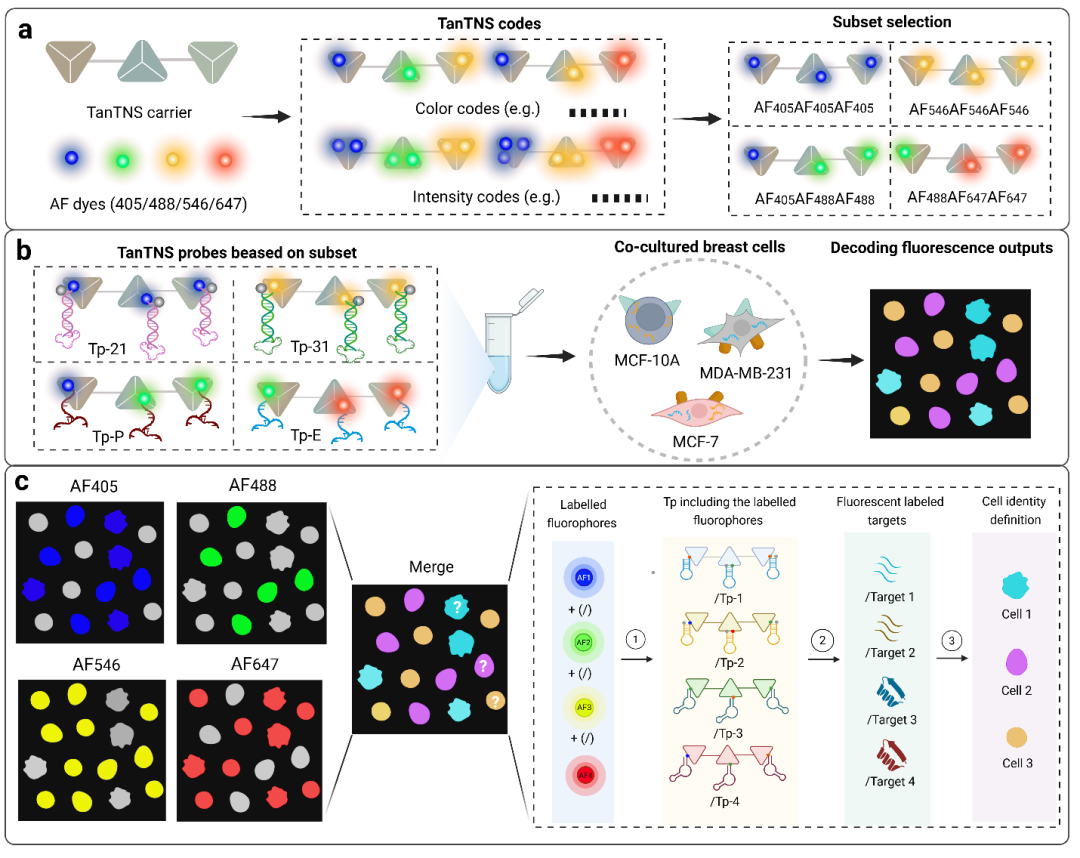
本研究将串联四面体DNA纳米线(Tandem shaped tetrahedral nano-string,TanTNS)作为荧光编码载体,通过调控Alexa Fluor染料的种类与数量,构建了容量超过2⁹种的颜色-强度复合编码库。研究人员结合编码结构与识别组件构建编码探针,能够对同一细胞系中两种miRNA(miR-21、miR-31)和两种膜蛋白(PTK7、EpCAM)实现多重荧光成像。基于不同乳腺细胞类型中的独特分子指纹,实现在混合细胞培养体系中三种乳腺细胞系的逻辑区分。此外,团队还开发了基于MATLAB的荧光共定位分析方法,用于验证双色探针信号的特异性并解码靶标的真实空间信息,为单细胞水平的多靶标空间信息解码提供了可靠工具。
亮点总结
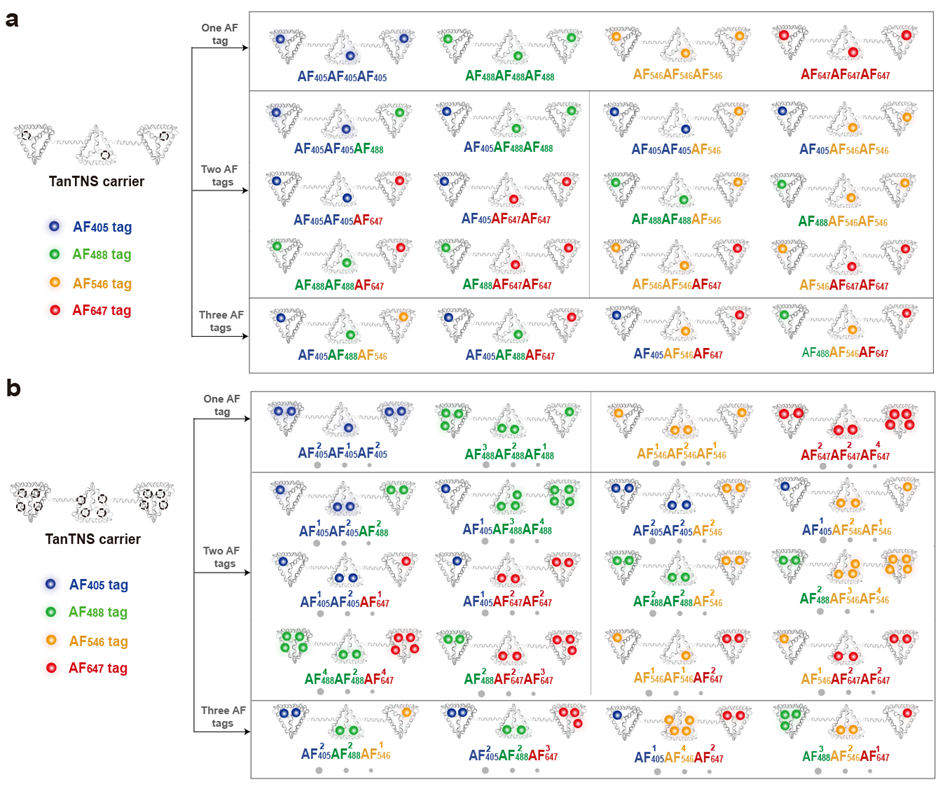
构建超高通量复合荧光编码库。以串联四面体DNA纳米线为载体,通过调控四种Alexa Fluor染料的种类与标记数量,构建了颜色-强度双维度编码体系,理论编码容量超过2⁹,突破了传统荧光编码通量受限的瓶颈。
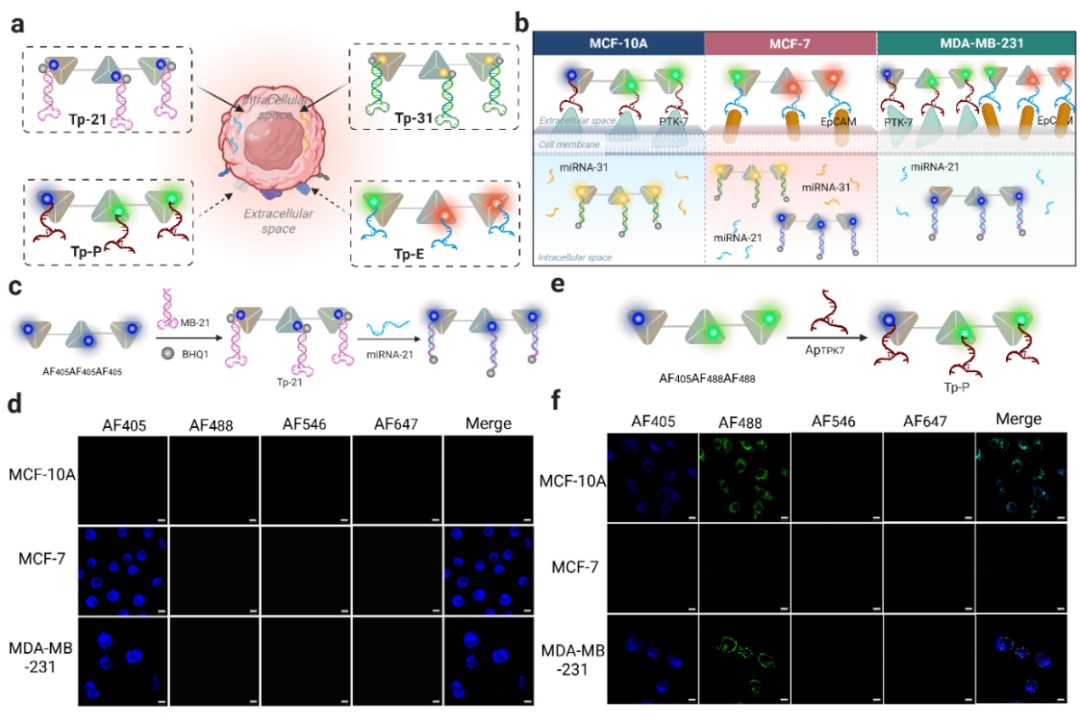
实现多类型生物标志物的同步原位成像。将编码结构分别与分子信标(靶向miRNA)和核酸适配体(靶向膜蛋白)偶联,成功在单细胞中同时成像两种miRNA和两种膜蛋白,展示了优异的靶标识别特异性和多重分析能力。
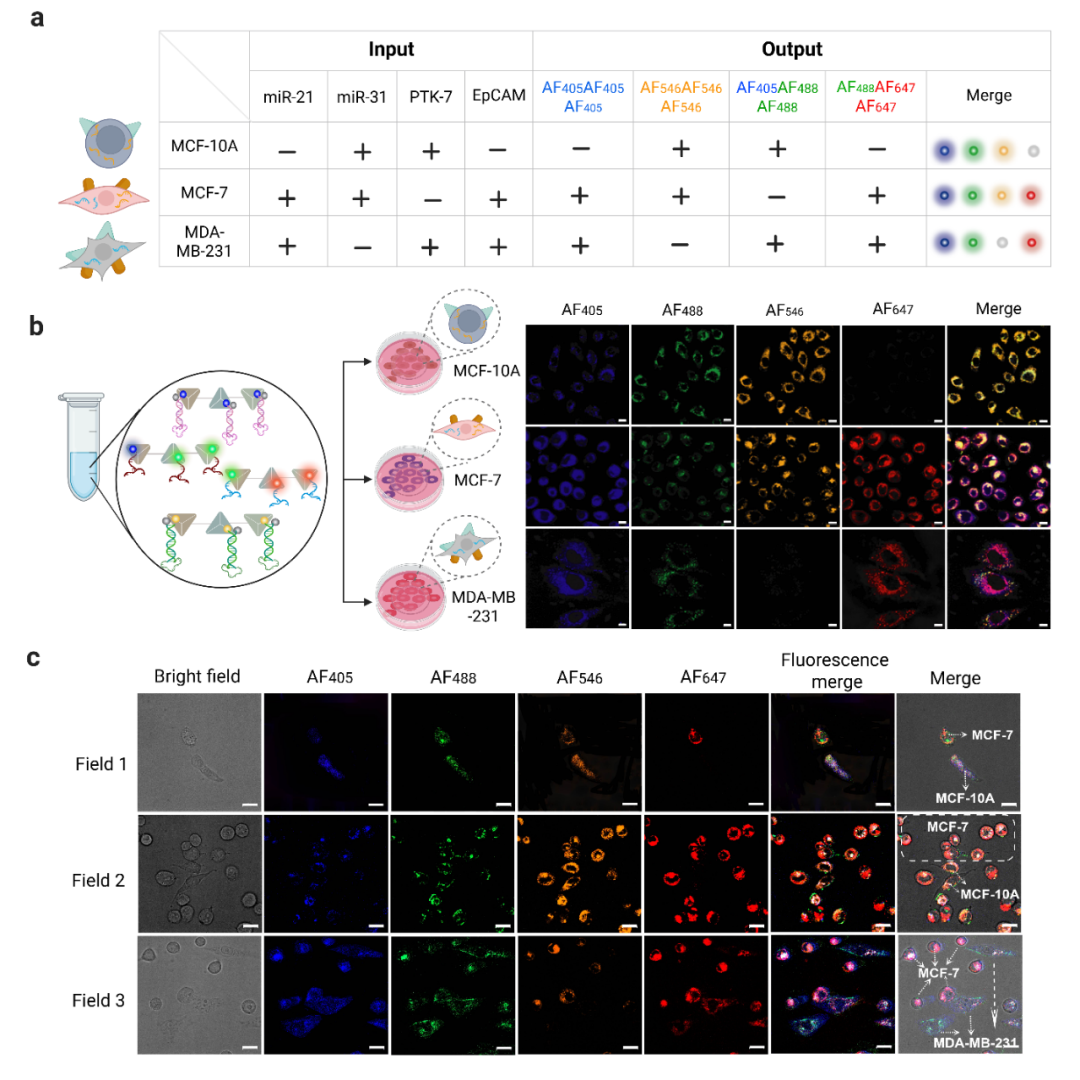
基于分子指纹逻辑区分混合细胞类型。利用三种乳腺细胞系中四种靶标的差异化表达谱,通过荧光伪彩组合即可直观识别细胞身份,无需复杂仪器即可实现混合细胞体系的精准区分。
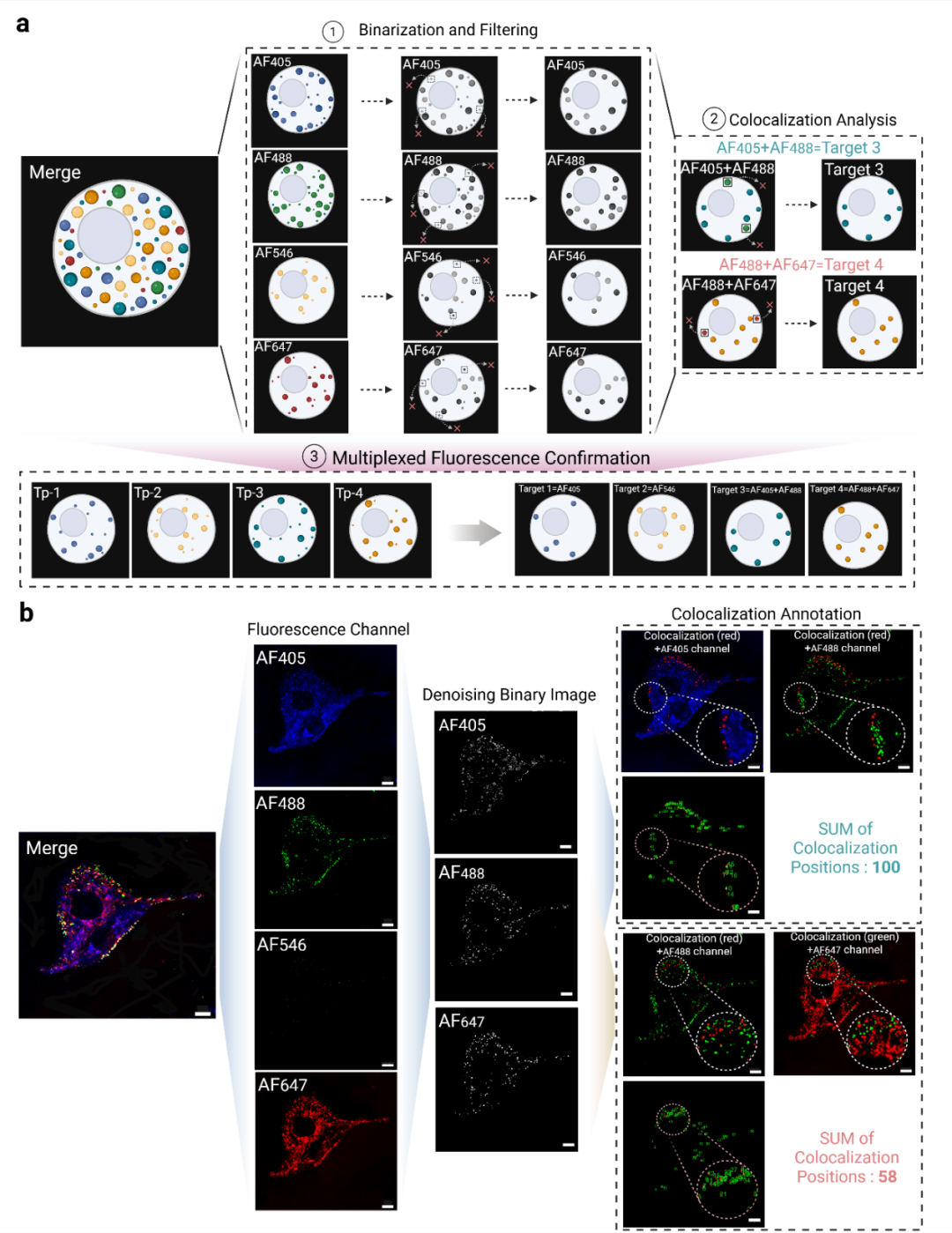
开发基于MATLAB的智能共定位解码算法。针对双色标记靶标,建立了灰度化、二值化、尺寸筛选及共定位识别的自动化分析流程,有效区分真实信号与背景噪声,实现了单细胞水平的精准空间解码,算法透明、可复现。
未来展望
更精细的乳腺癌分子分型。未来可通过引入更多光谱可分辨的荧光标签或结合其它编码维度,进一步扩大可使用的编码容量。在此基础上,拓展靶标种类,在单细胞层面实现更多亚群的一步式精准逻辑分型。
融合AI的图像解码与智能诊断决策系统。未来可将MATLAB共定位分析方法提升为基于深度学习的高通量、自动化荧光图像解码系统。将该系统与临床信息整合,构建能够预测药物响应、预后的智能诊断模型,为精准治疗提供辅助决策依据。
从科研工具到临床液体活检的转化。基于TanTNS探针体系,集成微流控芯片、自动化成像与智能解码算法,用于循环肿瘤细胞(CTC)或细胞外囊泡(EV)的多类型标志物逻辑分析,有望在复杂血液背景中高特异性鉴别乳腺癌来源的CTC亚型、监测复发与转移。
复旦大学人类表型组研究院宓现强教授为该研究通讯作者。博士后赵晓双为第一作者。复旦大学人类表型组研究院田梅教授、博士生高乙丹参与了该项研究。该项工作获得了国家重点研发计划等基金资助。
论文链接:https://doi.org/10.1016/j.mtbio.2026.103136






